���𰸡�
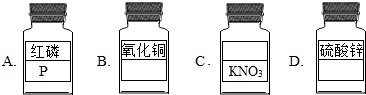
��������1������(j��)�����ﻯ�W(xu��)ʽ�ĕ������E���w��������(bi��o)�r(ji��)��������s�����M(j��n)�н��
��2������(j��)���ӵı�ʾ���������_�������|(zh��)�Ļ��W(xu��)ʽ����ʾ����(g��)ԓ���ӣ������仯�W(xu��)ʽǰ��������(y��ng)�Ĕ�(sh��)�֣��M(j��n)�н�𣻸���(j��)�x�ӵı�ʾ�������ڱ�ʾԓ�x�ӵ�Ԫ�ط�̖���Ͻǣ���(bi��o)��ԓ�x����������ؓ(f��)늺ɔ�(sh��)����(sh��)����ǰ����ؓ(f��)��̖�ں�1��(g��)늺ɕr(sh��)��1Ҫʡ�ԣ�����ʾ����(g��)ԓ�x�ӣ�������Ԫ�ط�̖ǰ��������(y��ng)�Ĕ�(sh��)�֣��M(j��n)�н��
����(j��)ԭ�ӵı�ʾ��������Ԫ�ط�̖����ʾһ��(g��)ԭ�ӣ���ʾ����(g��)ԓԭ�ӣ�������Ԫ�ط�̖ǰ��������(y��ng)�Ĕ�(sh��)�֣��M(j��n)�н��
����(j��)Ԫ�ػ��σr(ji��)�ı�ʾ�������_��������������Ҫ��(bi��o)����Ԫ�صĻ��σr(ji��)��Ȼ�����仯�W(xu��)ʽԓԪ�ص��Ϸ�����ؓ(f��)̖�͔�(sh��)�ֱ�ʾ����ؓ(f��)̖��ǰ����(sh��)���ں��M(j��n)�н��
��3���ٸ���(j��)�VȪˮ��(bi��o)����Ԫ�ط�̖�M(j��n)�н��
�ڸ���(j��)��(bi��o)��Ԫ�ط�̖���ϽǵĔ�(sh��)�ֱ�ʾ�x������늺ɔ�(sh��)���M(j��n)�н��
�۸���(j��)�քeӋ(j��)�㘋(g��u)�ɻ���������������|(zh��)���M(j��n)�б��^��
����⣺
��1������(j��)�����ﻯ�W(xu��)ʽ�ĕ������E���w��������(bi��o)�r(ji��)��������s�����ɵã�
�����~�Ļ��W(xu��)ʽ�飺CuO�� KNO
3 ���Q�飺����⛣� �����\�Ļ��W(xu��)ʽ�飺ZnSO
4��
�ʴ𰸞飺CuO������⛣�ZnSO
4��
��2������(j��)���ӵı�ʾ���������_�������|(zh��)�Ļ��W(xu��)ʽ����ʾ����(g��)ԓ���ӣ������仯�W(xu��)ʽǰ��������(y��ng)�Ĕ�(sh��)�֣����2��(g��)�����������ӱ�ʾ�飺2P
2O
5������(j��)�x�ӵı�ʾ�������ڱ�ʾԓ�x�ӵ�Ԫ�ط�̖���Ͻǣ���(bi��o)��ԓ�x����������ؓ(f��)늺ɔ�(sh��)����(sh��)����ǰ����ؓ(f��)��̖�ں�1��(g��)늺ɕr(sh��)��1Ҫʡ�ԣ�����ʾ����(g��)ԓ�x�ӣ�������Ԫ�ط�̖ǰ��������(y��ng)�Ĕ�(sh��)�֣����3��(g��)���F�x�ӱ�ʾ�飺3Fe
2+��
���̼����x�ӱ�ʾ�飺CO
32-��
����(j��)ԭ�ӵı�ʾ��������Ԫ�ط�̖����ʾһ��(g��)ԭ�ӣ���ʾ����(g��)ԓԭ�ӣ�������Ԫ�ط�̖ǰ��������(y��ng)�Ĕ�(sh��)�֣����һ��(g��)��ԭ�ӱ�ʾ�飺O��
����(j��)Ԫ�ػ��σr(ji��)�ı�ʾ�������_��������������Ҫ��(bi��o)����Ԫ�صĻ��σr(ji��)��Ȼ�����仯�W(xu��)ʽԓԪ�ص��Ϸ�����ؓ(f��)̖�͔�(sh��)�ֱ�ʾ����ؓ(f��)̖��ǰ����(sh��)���ں����ˮ����Ԫ���@-2�r(ji��)��ʾ�飺H
2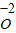
��
�ʴ𰸞飺2P
2O
5�� 3Fe
2+�� CO
32-�� O�� H
2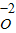
��
��3���ٸ���(j��)�VȪˮ��(bi��o)����Ԫ�ط�̖��֪�����У�Na��Ca��Cl��S��O��5�NԪ�أ��ʴ𰸞飺5��
�ڸ���(j��)��(bi��o)��Ԫ�ط�̖���ϽǵĔ�(sh��)�ֱ�ʾ�x������늺ɔ�(sh��)����֪Ca
2+�С�2���ĺ��x�ǣ�1��(g��)�}�x�ӎ�2��(g��)��λ����늺ɣ�
�ʴ𰸞飺1��(g��)�}�x�ӎ�2��(g��)��λ����늺ɣ�
��4�N���ӃɃɽY(ji��)���ܘ�(g��u)�ɵĻ������У�NaCl��CaCl
2��Na
2SO
4��CaSO
4��
NaCl �����������|(zh��)���飺23+35.5=58.5
CaCl
2 �����������|(zh��)���飺40+35.5×2=111
Na
2SO
4 �����������|(zh��)���飺23×2+32+16×4=142
CaSO
4 �����������|(zh��)���飺40+32+16×4=136
�ɴ˿�֪�����������|(zh��)�����Ļ�����Ļ��W(xu��)ʽ�飺Na
2SO
4��
�ʴ𰸞飺Na
2SO
4��
�c(di��n)�u�����}��Ҫ����W(xu��)�������W(xu��)���Z�ĕ����������������}Ŀ�O(sh��)Ӌ(j��)�Ȱ��������W(xu��)��̖���x���˽⣬�ֿ����ˌW(xu��)�������W(xu��)��̖�ĕ���������ȫ�棬ע�ػ��A(ch��)��


 ��
��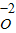 ��
��

 Ʒ�W(xu��)�p��(y��u)��ϵ�д�
Ʒ�W(xu��)�p��(y��u)��ϵ�д� С�W(xu��)��ĩ�_��100��ϵ�д�
С�W(xu��)��ĩ�_��100��ϵ�д� ��ĩ��(f��)��(x��)�z�yϵ�д�
��ĩ��(f��)��(x��)�z�yϵ�д�