
���}Ŀ��������a�����x���_���ٲ��ϣ�Ո�ÌW�^��֪�R�ش����І��}
(1)�����~����ԭ���������~��Һ�c�F�������䷴���Ļ��W����ʽ��_____���D1�~��Ʒ����;�У����ý��ٌ���Ե���_____(����ĸ)��
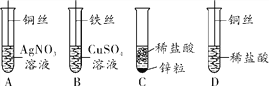
(2)���I�ϟ��F��ԭ��������һ����̼�������F������ij�dȤС�M���ÈD2�b���M��ԇՈ��Ҫ����գ�
�ٌ���CO߀ԭFe2O3�Ļ��W����ʽ_____������^�������^�쵽A�b���еĬF���_____����߅����ܿڷ����cȼ�ľƾ�����Ŀ����_____
���F��Ʒ��һ���l���������P�����ɵ��F�P������K��ӵ��F�^�m�c_____�������P������F��Ʒ�����Mһ���P�g���������ÏU�f������Ʒ��Ŀ��֮һ��_____��
���𰸡� Fe+CuSO4=FeSO4+Cu B 3CO+Fe2O3![]() 2Fe+3CO2 �t��ɫ��ĩ׃�ɺ�ɫ ̎��β�⣬��ֹ��Ⱦ�՚� ���⡢ˮ ���o�����YԴ
2Fe+3CO2 �t��ɫ��ĩ׃�ɺ�ɫ ̎��β�⣬��ֹ��Ⱦ�՚� ���⡢ˮ ���o�����YԴ
��������(1)�����~��Һ�c�F���������Ļ��W����ʽ�飺Fe+CuSO4=FeSO4+Cu�������~�Č�������Ƴ��~������(2)��CO߀ԭFe2O3�Ļ��W����ʽ��Fe2O3+3CO ![]() 2Fe+3CO2 �������F�Ǽtɫ���w�����ɵ��F�����s�|���ʬF��ɫ����A�b���еĬF���t��ɫ��ĩ׃�ɺ�ɫ����߅����ܿڷ����cȼ�ľƾ�����Ŀ����̎��β���е�һ����̼����ֹ��Ⱦ�՚⡣���F��Ʒ���P���F�c�՚��е�ˮ�����ͬ���õĽY�����F�P���ɶ�ף�������K��ӵ��F�^�m���P���������ÏU�f������Ʒ��Ŀ��֮һ�DZ��o�����YԴ��
2Fe+3CO2 �������F�Ǽtɫ���w�����ɵ��F�����s�|���ʬF��ɫ����A�b���еĬF���t��ɫ��ĩ׃�ɺ�ɫ����߅����ܿڷ����cȼ�ľƾ�����Ŀ����̎��β���е�һ����̼����ֹ��Ⱦ�՚⡣���F��Ʒ���P���F�c�՚��е�ˮ�����ͬ���õĽY�����F�P���ɶ�ף�������K��ӵ��F�^�m���P���������ÏU�f������Ʒ��Ŀ��֮һ�DZ��o�����YԴ��



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����һ������ʢ��22.3gNa2CO3��NaCl�M�ɵĹ��w��������109.1gˮ�ܽ⣬�Ƴ���Һ�������еμ����|�|���֔�10%��ϡ�}�ᣬ�ų����w�Ŀ��|���c������ϡ�}����|���Pϵ��D��ʾ��Ո�ش����}��

(1)�����l�������Ļ��W����ʽ_______________________��
(2)������֪�l���г�������ɚ��w�|��(X)�ı���ʽ_______________��
(3)���μ�ϡ�}�����DB�c�r����������Һ�����|���Q��_______________��
(4)���μ�ϡ�}�����DA�c�r���õ������Һ���˕r���ò����Һ�����|���|���֔���________________��
(5)�����|���֔�36.5%�ĝ���������146g����ϡ�}�ᣬ��Ҫ���}���ˮ���|����Ȟ�________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����D�黯�WС�M̽�����ٵĻ��W���|�������Ă����ش����І��}��
(1)������Һ׃�{�ķ����Ļ��W����ʽ______________________________��
(2)����������ܵó����ٵĻ���������__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��һ������ļtɫ��ĩ����Cu��Fe2O3��Fe(OH)3���N���w�е�һ�N��ɷN�M�ɡ�������ͬ�W����̽���^�̣�Ո�ㅢ�c���ش����P���}��
��������}��
����٣�ֻ��Cu ����ڣ�ֻ��Fe2O3
����ۣ�ֻ��Fe(OH)3 ����ܣ���Fe(OH)3��Fe2O3�Ļ����
����ݣ���Cu��Fe2O3�Ļ���� �������____�Ļ����
������Y�ϡ�
��1��2Fe(OH��3![]() Fe2O3+3H2O
Fe2O3+3H2O
��2��Cu�ܽ���Fecl3��Һ�У��õ�FeCl2��CuCl2
[���̽��]
��3����ͬ�W�M�����Ќ�Ո������пհ�̎��
���������E | ���F�� | �YՓ |
��ȡ�������tɫ���w������ԇ���мӟ� | ���w�]�����@׃����ԇ�ܿڸ����ȱڛ]�аl�FСҺ�� | �tɫ���w����________ |
��ȡ�����tɫ��ĩ��ԇ���У��μ�������ϡ�}�� | �l�F���wȫ���ܽ⣬��Һ׃ɫ | ����_____���ܳ������������漰�Ļ��W��������ʽ��___ |
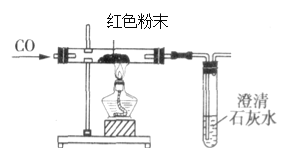
��4���ڼ�ͬ�W���Ļ��A�ϣ���ͬ�W���Mһ���_���tɫ��ĩ�ĽM�ɣ��Qȡԓ��ĩ10.0g�b��Ӳ�|�������У����҈D�b���M�Ќ����r�l�F����ʯ��ˮ׃���ᣬ�C���tɫ��ĩ�к���Fe2O3Ӳ�|�������аl�������Ļ��W����ʽ��______������ȫ��y��ʯ��ˮ�|������6.6g(�ٶ�CO���࣬ʯ��ˮ�������a�����wȫ��������)�tՈӋ���ԓ�tɫ��ĩ�и��ɷֵ��|��____
����˼�u�r����ͬ�Wָ�����ĭh���Ƕȣ���ͬ�W�Č���b���Ї��ز���֮̎��Ո�����ľ��w���M��ʩ��ԭ��________________
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���D��A��B��C��D�dz��л��W��Ҋ���ķN���|������A��B�ǽM��Ԫ����ͬ�ăɷN��B�����C��t��ɫ���w��D����|����������ʾ���B�ɷN���|�ܰl�����W��������������ʾ���|�g���D���Pϵ(���ַ���������P�����l����ʡ��)��Ո�ش���
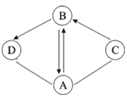
(1)D�Ļ��Wʽ��_________��
(2)A+C�����Ļ��W����ʽ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���^�����ጦ�����Ͳ������и�Ч�����ٚ������ã��ڿ������ǵ��ͷ��ס��đ����б��V�������ڭh������������D���^ ������ĽY��ʽ���������P�^������Ĕ����в����_����( )

A. �^��������ӵĻ��Wʽ��C2H4O3 B. �^����������������|����76
C. �^�������К�Ԫ�ص��|���֔���� D. ��ȫȼ������H2O��CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��ij���W�W��С�M���������b��(�A���b������)�����Pԇ�����Ԝy���՚���O2���w�e�ٷ֔���
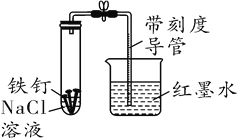
(1)���ǰ��10%��H2SO4��Һ��ϴ�F����К��ݮa������H2SO4��Һ��ϴ��Ŀ����__________���������P���W����ʽ______________________________��
(2)��֪ԇ��ʣ����g�͌��ܵ��w�e��40 mL�����ܽ���e�s��1 cm2���γɷ���Һ���r���xȡ�x����8.2 cm���t�՚���������w�e�֔���______%��
(3)���r�l�F�����y���^�����^���ĕr�^�L������Ӱ����������·�����
��������O�����Oһ����Һ��pH��ͬ��
���O����NaCl��Һ�ĝ�Ȳ�ͬ��
Ո�������һ�N���O�����O����______________________________��ͬ��
���M�Ќ�������������b�ã�ͨ�^ȡ�w�e�������ͬNaCl��Һ�{����Һ��pH�@������������
pH | 2.0 | 5.5 | 6.0 | 6.5 | 7.0 | 8.0 |
Һ���߶�(cm) | 0 | 1.3 | 8.2 | 8.2 | 8.2 | 8.2 |
�γɷ���Һ���r�g(min) | 3.0 | 3.0 | 5.1 | 5.3 | 15.6 | 17.5 |
�����YՓ������������������s�̌��y���r�g��pH����ѷ�����____________��
����˼����pH��2�r���]���^�쵽����Һ���γɵ�ԭ����________________��
��ע�⣺��������_�ش����І��}��������4�֣������Wԇ�����ֲ����^60�֡�
Ո���OӋ��̽��NaCl��Һ�ĝ�Ȍ��F���P���ʵ�Ӱ푡�
���E�� __________________________________________________________��
���F��________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�����ʏS���a�ϳɰ���ԭ����ú���՚⡢ˮ�����a��Ҫ�������£�
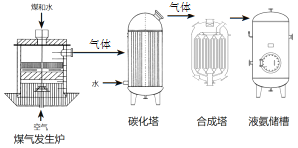
��֪����ú��l���t����Ҫ�����У�
��C+O2 ![]() CO2�� ��C+H2O
CO2�� ��C+H2O![]() CO+H2
CO+H2
���ϳɵİ��ⲿ��ͨ��̼�������ȳ�ȥ�˶�����̼�ֵõ��˻���NH4HCO3�����f�����_����
A. ԓ�ϳɰ���ˇ�ĮaƷֻ��Һ����̼����@
B. �����д̼��Ԛ�ζ����ʹ���{ɫʯ��ԇ��׃�t
C. ú��l���t��횱����^�ߵĠt��
D. ̼�����аl�������ķ���ʽ���Ա�ʾ��NH3+H2O+CO2=NH4HCO3�����Ȝضȑ��^��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�����W�������a�������_�������ĸ������뻯�W�����ö����ķ����о��՚�ɷ֣�����һ헌����Ǽӟ���������ĩ�õ��˹������⣨�^ʾ��D���£��������f�����_���ǣ� ��
![]()
A��ԓ�����f�������|����ԭ���|��С
B��ԓ������������c�՚��е����⻯�W���|��ͬ
C��ԓ�����f��ԭ�ӵĔ�Ŀ�ڻ��W����ǰ���ǰl��׃����
D��ԓ�����f��Ԫ�صķN��ڻ��W����ǰ���ǰl����׃��
�鿴�𰸺ͽ���>>
���H�WУ���x - �������б� - ԇ�}�б�
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^ | ����p�_�e�^ | ��vʷ̓�o���x�к���Ϣ�e�^ | �����֙��e�^
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com