
【題目】已知A為化合物,且其摩爾質量為95g·mol-1,D為混合物,M是一種常見的氣體,N是一種常見金屬單質。它們之間的轉化如圖所示。
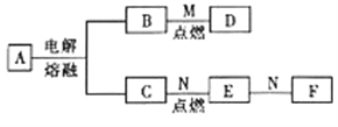
請回答下列問題:
(1)A的化學式為___________。
(2)由A生成B和C的反應中,每轉移1mol電子,可以生成________gB。
(3)已知D中含有兩種固體,且其中有一種固體單質為黑色,另一種固體為B的氧化物。則M的摩爾質量為_________g·mol-1。
(4)E的水溶液與N反應的離子方程式為___________________________。
【答案】 MgCl2 12 44 2Fe3++Fe=3Fe2+
【解析】試題分析:鎂在二氧化碳氣體中燃燒生成氧化鎂和碳單質,D中含有兩種固體,且其中有一種固體單質為黑色,另一種固體為B的氧化物,所以D是氧化鎂和碳單質、B是鎂;氯化鎂的摩爾質量是95g·mol-1,電解熔融氯化鎂生成鎂和氯氣;鐵在氯氣中燃燒生成氯化鐵,氯化鐵和鐵反應生成氯化亞鐵。
解析:根據以上分析,(1)A是氯化鎂 ,化學式為MgCl2。
(2)由氯化鎂電解生成鎂和氯氣的反應中,鎂由+2價變為0價,每轉移1mol電子生成0.5mol鎂,質量是12g。
(3)根據以上分析,M是二氧化碳,摩爾質量為44g·mol-1。
(4)E是氯化鐵,氯化鐵溶液與鐵反應生成氯化亞鐵的離子方程式為2Fe3++Fe=3Fe2+。


科目:高中化學 來源: 題型:
【題目】已知: ![]() 溶液是檢驗
溶液是檢驗![]() 的試劑,若溶液中存在
的試劑,若溶液中存在![]() ,將產生藍色沉淀。將
,將產生藍色沉淀。將![]() 的KI溶液和
的KI溶液和![]()
![]() 溶液等體積混合后,取混合液分別完成下列實驗,能說明溶液中存在化學平衡“
溶液等體積混合后,取混合液分別完成下列實驗,能說明溶液中存在化學平衡“![]() ”的是
”的是
實驗編號 | 實驗操作 | 實驗現象 |
① | 滴入KSCN溶液 | 溶液變紅色 |
② | 滴入 | 有黃色沉淀生成 |
③ | 滴入 | 有藍色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液變藍色 |
A. ① B. ②和④ C. ③和④ D. ①和②
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在給定的條件下,下列選項所示的物質間轉化均能實現的是( )
A. NaCl(aq)![]() NaHCO3(s)
NaHCO3(s)![]() Na2CO3(s)
Na2CO3(s)
B. FeS2![]() SO2
SO2![]() H2SO4
H2SO4
C. SiO2![]() SiCl4
SiCl4![]() Si
Si
D. N2![]() NH3
NH3![]() NH4Cl(aq)
NH4Cl(aq)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用電解法可提純含有某些含氧酸根雜質的粗KOH溶液,其工作原理如圖所示。下列有關說法錯誤的是
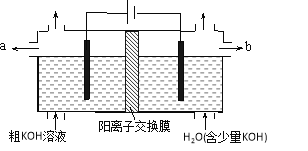
A. 通電后陰極區附近溶液pH會增大
B. 陽極反應式為4OH--4e-=2H2O+O2↑
C. 純凈的KOH溶液從b出口導出
D. K+通過交換膜從陰極區移向陽極區
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】查閱資料:元素鉻(Cr)在溶液中主要以Cr3+(藍紫色) 、Cr(OH)4-(綠色) 、Cr2O72(橙紅色)、CrO42(黃色)等形式存在,Cr(OH)3為難溶于水的灰藍色固體,回答下列問題:
(1)鉻(24Cr)屬于________(選填編號)。
a.主族元素 b.副族元素 c.Ⅶ族元素 d.過渡元素
(2)CrO42和Cr2O72在溶液中可相互轉化。室溫下,初始濃度為1.0 mol·L1的Na2CrO4溶液中c(Cr2O72)隨c(H+)的變化如圖所示。
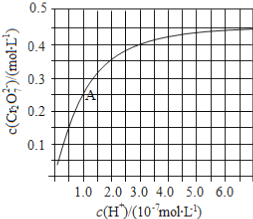
①用離子方程式表示Na2CrO4溶液中的轉化反應____________。
②由圖可知,溶液酸性增大,CrO42的平衡轉化率__________(填“增大“減小”或“不變”)。根據A點數據,計算出該轉化反應的平衡常數為__________。
③升高溫度,溶液中CrO42的平衡轉化率減小,則該反應的ΔH_________0(填“>”“<”或“=”)。
(3)欲降低廢水中重金屬元素鉻的毒性,可將Cr2O72-轉化為Cr(OH)3沉淀除去.已知:
氫氧化物開始沉淀時的pH | 氫氧化物沉淀完全時的pH | |
Fe2+ | 7.0 | 9.0 |
Fe3+ | 1.9 | 3.2 |
Cr3+ | 6.0 | 8.0 |
某含鉻廢水處理的主要流程如圖所示:
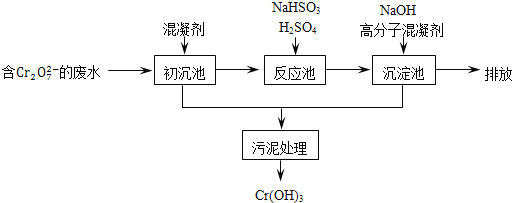
①初沉池中加入的混凝劑是K2SO4﹒Al2(SO4)3﹒24H2O,其作用為__________(用離子方程式表示).
②反應池中用NaHSO3將酸性廢液中的Cr2O72-還原成Cr3+,該反應的離子方程式為________.根據“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此過程中發生主要反應的離子的先后順序是____________.證明Cr3+沉淀完全的方法是__________.
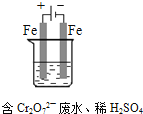
(4)工業可用電解法來處理含 Cr2O72-廢水.實驗室利用如圖模擬處理含Cr2O72-的廢水,陽極反應式是Fe-2e-═Fe2+,陰極反應式是2H++2e-═H2↑.Fe2+與酸性溶液中的Cr2O72-反應的離子方程式是__________,得到的金屬陽離子在陰極區可沉淀完全,用電解法處理該溶液中0.01mol Cr2O72-時,至少得到沉淀的質量是__________ g.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學設計如圖所示實驗測量m g銅銀合金樣品中銅的質量分數:
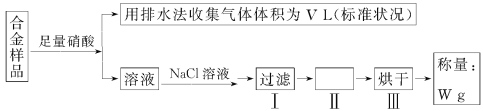
下列說法中不正確的是 ( )
A. 收集到的V L氣體全為NO
B. 過濾用到的玻璃儀器:燒杯、漏斗、玻璃棒
C. 操作Ⅱ應是洗滌
D. 銅的質量分數為![]() ×100%
×100%
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com