
���}Ŀ���ס�����Ԫ�����ڱ���ͬһ����ăɷNԪ�أ�����ԭ���� x���t�ҵ�ԭ����������
A. x��2 B. x+4 C. x+8 D. x+18
���𰸡�B
��������
��Ԫ�����ڱ��Y��������̎�ڢ�A����AԪ�ض��ԣ���ͬ�������������Ԫ�ص�ԭ����ֵ��ͬ������̎����������Ԫ�ض��ԣ���ͬ�������������Ԫ�ص�ԭ����ֵҲ��ͬ��
��Ԫ�����ڱ��Y��������̎�ڢ�A����A Ԫ�ض��ԣ�ͬ����ԭ���� ��֮�����һ����Ԫ�صķN��������������壬ͬ����ԭ����֮�����һ����Ԫ�صķN���ͬһ���岻ͬ���ڵ�Ԫ�أ�ԭ���������ܞ�2��8��18��32�Ȼ������ĽM�ϣ����������4������ԭ�������ܞ�x+4�����xB��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� С�W��10��犑����}ϵ�д�
С�W��10��犑����}ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�����I�ϳ����ú���Uˮ���a Na2S2O3��5H2O������ҿ�����D�b��(��ȥ���֊A�փx��)ģ�M���a�^��
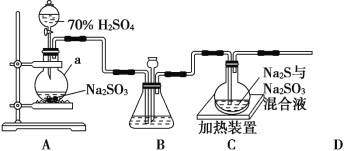
(1)�x��a�����Q��__________��A�аl���Ļ��W�������̞�_______________________��
(2)����У���ʹ SO2 �����M���b��C�����õIJ���______________���b��C���Ƃ䷴���Y���ĬF��___________________��
(3)�b�� C �е���Һһ��������ډA�ԭh������t�aƷ�l�S�����x�ӷ���ʽ��ʾ��ԭ��� ___________________��
(4)��p���b��C�п��ܳ��F��Na2SO4�s�|���ڲ���׃ԭ���b�õĻ��A�ϑ���ȡ�IJ�����__________________��
(5)�b�� D ����̎��β�⣬���x�õ�������b��(�A�փx������ȥ)��_____(����̖)��

�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���о�NO2��NO��CO����Ⱦ���̎�팦���O�����Ї�������Ҫ���x��
��1�����ü����߀ԭNOx��
CH4(g)+4NO2(g) ===4NO(g)+CO2(g)+2H2O(g) ��H1����574 kJ��mol-1
CH4(g)+4NO(g) ===2N2(g)+CO2(g)+2H2O(g) ��H2����1160 kJ��mol-1
�ټ���ֱ�ӌ�NO2߀ԭ��N2�ğữ�W����ʽ��________________________________��
�ڌ�CH4��NO2�������]�����аl������������ԓ�����_��ƽ�������߷������ʵ�ͬ�r���NO2���D���ʣ��ɲ�ȡ�Ĵ�ʩ��__________(��һ�c����)��
������ԭ늳ط����Ɍ��FNO2�ğo��������������6NO2+8NH3===7N2+12H2O��늽��|��Һ��NaOH��Һ������һ�Εr�g��ԓ늳����O�^������ҺpH________(��������pС����׃��)��ؓ�O��늘O����ʽ��___________________��
��2�����(COCl2)�����ϡ��Ƹ��ˎ�ȹ��I�����S����;�����I�ϳ����ÏU��CO2ͨ�^������C(s)+CO2(g)![]() 2CO(g) ��H>0����ȡ�ϳɹ���ԭ�Ϛ�CO�����w�e��׃�ĺ㉺(p��)���]�����г���1mol CO2 �c������̼�l��������������ƽ��r�wϵ�К��w�w�e�֔��c�ضȵ��Pϵ��D��ʾ��
2CO(g) ��H>0����ȡ�ϳɹ���ԭ�Ϛ�CO�����w�e��׃�ĺ㉺(p��)���]�����г���1mol CO2 �c������̼�l��������������ƽ��r�wϵ�К��w�w�e�֔��c�ضȵ��Pϵ��D��ʾ��
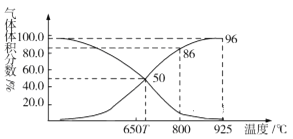
��T��r����������������ϡ�К��w��ƽ��______�Ƅ�(���������������ͬ)����������w�e��CO2��CO��ƽ��________�Ƅӡ�
��CO�w�e�֔���40%�r��CO2���D���ʞ�_______��
����֪�����w�։�(p��)=���w�������w�e�֔���800��r��ƽ��։�����ƽ���ȱ�ʾƽ�ⳣ��Kp=______(�ú�p���Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���ڃɂ����ݵ����]�������M�����Ѓɂ����淴����
����C(s)��H2O(g)![]() CO(g)��H2(g)
CO(g)��H2(g)
����CO(g)��H2O(g)![]() CO2(g)��H2(g)
CO2(g)��H2(g)
�F�����Р�B���ٻ�Ϛ��wƽ�����������|�����ٸ�׃
�ں�ؕr�����w�������ٸ�׃���۸����w�M�ɝ�����
�ܷ����wϵ�Мضȱ��ֲ�׃���ݔ��њ����I�����ǔ��њ���I���ʵ�2������Ϛ��w�ܶȲ�׃���߆�λ�r�g�ȣ�����ˮ�����|���c���ɚ���|���Ȟ�9��1
�����ܱ����ס��������з������_��ƽ���B����(����)
A. �٢ڢ� B. �ۢܢ� C. �ޢ� D. �ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��Cr��Fe��Ni���|������������Ҫ����;��
��1����Cr2O3��ԭ�ϣ��X����߀ԭ�����X�ᷨ�����a�����t����Ҫ����֮һ��ԓ������һ���l�şᷴ�����ɴ˿��Д�Cr��O�I��Al��O�I��____________�I�������о��l�F��B�Ȼ��X(Al2Cl6)�Ǿ�����λ�I�Ļ���������ڷǘO���܄����ɴ˿�֪ԓ������______(��O�ԡ��ǘO�ԡ�)�ġ�
��2���F�Ц����á������N���w���ͣ����Ц���Fe���|���w���������w���ģ�Fe���|�麆���������w���t�@�ɷN���w�Y�����Fԭ�ӵ���λ��֮����______��
��3��FeS2���w�ľ������D��ʾ������߅�L��a nm��FeS2����ʽ����M�������ӵ��_������ֵ��NA���侧�w�ܶȵ�Ӌ����_ʽ��___________g��cm3��������Fe2+λ��S22�����γɵ��������w���w�ģ�ԓ�������w��߅�L��______nm��

��4����������ڰ�ˮ�γ�[Ni(NH3)6]SO4�{ɫ��Һ��
��[Ni(NH3)6]SO4����x�ӵ����w������__________��
����[Ni(NH3)6]2+��Ni2+�cNH3֮�g�γɵĻ��W�I�Q��__________���ṩ����ӌ��ij��Iԭ����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����֪���W������:Fe(s)+CO2(g)![]() FeO(s)+CO(g),�仯�Wƽ�ⳣ����K1;���W������:Fe(s)+H2O(g)
FeO(s)+CO(g),�仯�Wƽ�ⳣ����K1;���W������:Fe(s)+H2O(g)![]() FeO(s)+H2(g),�仯�Wƽ�ⳣ����K2,�ڜض�973 K��1173 K����r��,K1��K2��ֵ�քe����:
FeO(s)+H2(g),�仯�Wƽ�ⳣ����K2,�ڜض�973 K��1173 K����r��,K1��K2��ֵ�քe����:
�ض� | K1 | K2 |
973 K | 1.47 | 2.38 |
1 173 K | 2.15 | 1.67 |
(1)ͨ�^�����еĔ�ֵ�����Ɣ�:��������_______(���������������ş���)������
(2)�F�з�����:CO2(g)+H2(g)![]() CO(g)+H2O(g),Ո�㌑��ԓ������ƽ�ⳣ��K3�ı��_ʽ:K3=______��
CO(g)+H2O(g),Ո�㌑��ԓ������ƽ�ⳣ��K3�ı��_ʽ:K3=______��
(3)�����������c�ڿ��ƌ���K1��K2�cK3֮�g���Pϵʽ��__________,�����Pϵʽ���ϱ픵��,���Ɣ����������________(���������������ş���)������
(4)Ҫʹ��������һ���l���½�����ƽ���������������Ƅ�,�ɲ�ȡ�Ĵ�ʩ��______ ��_____ (���ĸ��̖)��
A.�sС�����������ݷe B.�U���������ݷe
C.���ߜض� D.ʹ�ú��m�Ĵ���
E.�O���pСƽ���wϵ�е�CO�ĝ��
(5)�D�ס��ҷքe��ʾ��������t1�r���_��ƽ��,��t2�r�����׃ij���l�����l��׃������r:

�وD����t2�r�̰l����׃�ėl����__________��
�ڈD����t2�r�̰l����׃�ėl����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���������|���ڼ�������� �� ��
A.�����Ŀ՚�B.ʳ�}ˮC.���б��K��ˮD.��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��X��Y��Z��W�����ķN������Ԫ�أ����P�����IJ��ֽY����Ϣ�����|��Ϣ�����ʾ��
Ԫ�� | ���ֽY����Ϣ | �������|��Ϣ |
X | X�Ć��|���pԭ�ӷ��Ә��� | X�Ě仯��ˮ��Һ�ʉA�� |
Y | Yԭ�ӵ��������Ӕ�����Ȍ���Ӕ��ăɱ� | Y���γɶ�N��B�仯�� |
Z | Zԭ����������ӌ� | ����ZԪ�صĻ��������ɫ�������Sɫ |
W | Wԭ�ӵ��������Ӕ�����(2n��1)(n��ԭ�Ӻ�����ӌӔ�) | W��Z�ܰ�1��1��ԭ�ӂ������γ��x�ӻ����� |
Ո��Ҫ��ش����І��}��
(1)W��Ԫ�����ڱ��е�λ����______��
(2)X���Κ�B�仯��ķ���ʽ��______��(�û��Wʽ��ʾ)
(3)X��Y��W���NԪ�ص���߃r�������ˮ����������ɏ������������______��(�û��Wʽ��ʾ)
(4)Z���|��W���|�аl�������Č��F����______��
(5)����W�Ć��|�c��������Ļ�Ϛ��wͨ��ˮ�����l���������x�ӷ���ʽ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���Ć��|�ͻ������ڿ����c���a�����S����Ҫ��;���~����Ͻ����������ʹ�õĽ��ٲ��ϡ�Ո�ش����І��}:
(1)��������һ�N���|������ӽY����D��ʾ���tһ����������____�����I��ӌ���____������ӌ���

(2)N��P����+5�r��PCl5���γ��x���;��w�������к���[PCl4]+��[PCl6]�����t[PCl4]+���g���͞�______��
(3)�ؓ�Ա��^:P_____S(�>����=����<��)����P�ĵ�һ��x�ܱ�S���ԭ����______��
(4)�~����Ͻ����������ʹ�õĽ��ٲ��ϣ�Cu2+���cNH3�γ���λ����4�������[Cu(NH3)4]SO4��
���~Ԫ�������ڱ��е�λ����__________ ��1mol[Cu(NH3)4]SO4 ��___mol��λ�I ����[Cu(NH3)4]SO4�У����ڵĻ��W�I�������_____(���̖)��
A���x���I B�������I C����λ�I D���ǘO���I E���O���I
(5)���(GaP)���������������������������������Ͱ댧�w���ϡ�GaP�ľ��w�Y�����W�\�V�ͽY��(��D��ʾ)����������apm��
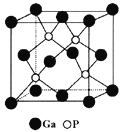
���cGa�o����P������________��
��GaP���w���ܶȞ�(�г�Ӌ��ʽ) ______g��cm��3(NA�鰢���ӵ��_����)��
�鿴�𰸺ͽ���>>
���H�WУ���x - �������б� - ԇ�}�б�
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^ | ����p�_�e�^ | ��vʷ̓�o���x�к���Ϣ�e�^ | �����֙��e�^
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com