
���}Ŀ���������Ќ������ͬF�����ó��ĽYՓ���_����
�x� | �������ͬF�� | �YՓ |
A | �������м�������ᣬ����ú�ɫ���d����w�����ų��̼��Ԛ�ζ���w | ������H�w�F��ˮ�Ժ�Óˮ�� |
B | ���{ɫʯ��ԇ���ϵμ�������ˮ��ԇ��߅���ʼtɫ�����g���ɫ | ��ˮ������������߀ԭ�� |
C | �u���NY�cNaOH��Һ�����������ϡ���ᣬ�ٵμ�AgNO3��Һ���a����ɫ���� | �u���NY�к�����ԭ�� |
D | ȡ5 mL 0.1 mol��L��1KI��Һ������1 mL 0.1 mol��L��1FeCl3��Һ����ȡ��Һ����ˮ�ӵ���KSCN��Һ����Һ׃��Ѫ�tɫ | Fe3���cI�����l���ķ�������淴�� |
A. A B. B C. C D. D
���𰸡�CD
��������
A. �����м��������ú�ɫ��̿���f�����������Óˮ�ԣ��ų��Ĵ̼��Ԛ�ζ���w��SO2���f����������Џ������ԣ�C+2H2SO4(��)![]() CO2��+SO2��+2H2O��A��e�`��
CO2��+SO2��+2H2O��A��e�`��
B. ԇ��߅���ʼtɫ���f����ˮ�@���ԣ�Һ�����g���ɫ���f��Һ�����g��HClO��ȴ�HClOƯ����ԇ�����f����ˮ����Ư���ԡ�B��e�`��
C.�u���N��NaOH��Һ�аl��ˮ�ⷴ��R-X+NaOH![]() R-OH+NaX����������ϡ�����к��^����NaOH���ټ���AgNO3��ҺAg++X-=AgX�����ɵİ�ɫ������AgCl������Y���ȴ��N��C����_��
R-OH+NaX����������ϡ�����к��^����NaOH���ټ���AgNO3��ҺAg++X-=AgX�����ɵİ�ɫ������AgCl������Y���ȴ��N��C����_��
D.�з���2I-+2Fe3+=I2+2Fe2+�� 5 mL 0.1 mol��L��1KI��Һ�c1 mL 0.1 mol��L��1FeCl3��Һ�����|����֮��n(KI):n(FeCl3)��5:1���f��KI�^�������ԓ�����Dz����淴�����t��Ϻ���Һ�Л]��Fe3+����ȡ��Һ���ˮ���м���KSCN��Һ����Һ����׃�t����������Һ׃�t������Fe3���cI�����l���ķ�������淴����D����_�����xCD��



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��ij�ضȕr����2L������X��Y��Z���N���|�S�r�g��׃���Pϵ������D��ʾ��

��1���ɈD�еĔ���������ԓ�����Ļ��W����ʽ��____________________________________________
��2�������_ʼ��2min��5minZ��ƽ���������ʞ�__________________��_______________��
��3��5min��Z���������ʱ�5minĩZ�� ��������___________����С����ȣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��ij���W�dȤС�M�y�����F�V����Ҫ�ɷ�FeS2���V������Ԫ�ص��|���֔����M��������m1g��Ʒ������D��ʾ�b��C�У����_K1�P�]K2����a̎����ͨ��՚⣬�ߜ��Ɵ�ʯӢ���еĘ�Ʒ��

Ո�ش����І��}��
��1���b��B�����Q��_____��a̎����ͨ��՚��Ŀ����_____��
��2���b��A��������_____��
��3�������Y�����P�]K1���_K2�����ƿ�м���Һ�w���cȼG̎�ƾ�����ʹ��ƿ�з����l��������������D��

�ٲ���I������Һ�����������|��_____��
�ڲ�������ϴ�졢��ɡ��Q�أ��z���w�Ƿ�ϴ���ķ�����_____��
��ԓ���F�V����Ԫ�ص��|���֔���_____���ú�m1��m2�Ĵ���ʽ��ʾ��
��4��ȡ�џ��������������Fe2O3��FeO��������C���д���FeO�����x�õ�ԇ����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��X��Y��Z��W��R����N����������Ԫ�أ���ԭ������������X�cWͬ���壬Z�cRͬ���壬X��ԭ�Ӱ돽��Y��С��Y����߃r���������ˮ�����Ǐ��ᣬZ���������Ӕ�����Ȍ���Ӕ���3���������f�����_����
A. ԭ�Ӱ돽��r(W)>r(Z)>r(Y)
B. ���Κ�B�仯��ğ᷀���ԣ�Y>Z
C. R�����������ˮ������鏊��
D. W2Z2�cX2R������r�I
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���Ҝ��£���0.100 0 mol��L��1NaOH��Һ�ζ�20.00 mL 0.050 0 mol��L��1H2C2O4��Һ���õζ�������D��ʾ�������P����Һ���������|��������Pϵһ�����_����

A. �������ζ��^���У�ʼ�K���ڣ�c(H��)�� c(Na��) ��c(OH��)��c(C2O42-)�� c(HC2O4-)
B. ��V[NaOH(aq)]��10.00 mL�r��c(Na��)> c(HC2O4-)>c(C2O42-)> c(H2C2O4)
C. ��V[NaOH(aq)]��15.00 mL�r��3c(Na��)�� 2c(C2O42-)�� 2c(HC2O4-)��2c(H2C2O4)
D. �� V[NaOH(aq)]��30.00 mL�r��c(C2O42-)��2c(HC2O4-)��3c(H2C2O4)��c(OH��)��c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
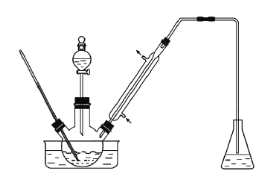
���}Ŀ��������Ա���ȩ��ԭ���Ƃ��g�屽��ȩ������b��Ҋ�D�����P���|�ķ��cҊ��������
���| | ���c/�� | ���| | ���c/�� |
�� | 58��8 | 1��2-�������� | 83��5 |
����ȩ | 179 | �g�屽��ȩ | 229 |
�䌍�E�飺
���E1�������iƿ�е�һ����ȵğoˮAlCl3��1��2����������ͱ���ȩ��ֻ�Ϻ�������60�棬�����μӽ�����������^��Һ�壬���ط���һ�Εr�g����s��
���E2������������マ������һ������ϡ�}���У����衢�o�á���Һ���ЙC����10%NaHCO3��Һϴ�졣
���E3����ϴ����ЙC������m���oˮMgSO4���w������һ�Εr�g���^�V��
���E4���p�����s�ЙC�࣬�ռ������s�֡�
(1) ����b���������ܵ���Ҫ������___________________��
(2) ���E1����������|�У���һ�N���|�Ǵ������仯�Wʽ��__________________
(3) �����ɱ���ȩ��ȡ�g�屽��ȩ�Ļ��W����ʽ_____________________________________________________
(4) ���ֹ��Ⱦ�h�����F��ƿ��ʢ�b����Һ��ԓ��______________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����������߀ԭ������2Ag+ (aq) + Cu(s) == Cu2+ (aq) + 2Ag (s)�OӋ��ԭ늳����D��

Ո�ش����І��}��
��1��늘OX�IJ�����____________��늽��|��ҺY��_____________��
��2���y늘O��늳ص�_________�O���y늘O�ϰl����늘O����ʽ______________��
��3�����·�е�����Ǐ�________늘O����______늘O����늘O�IJ��ϣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���ڲ�ͬ�ض��£���V L���]�����м���0.5 mol NO��0.5 mol����̿���l��������
2NO(g)+C(s)![]() N2(g)+CO2(g) ��H= ��Q kJ��mol-1(Q>0)���_��ƽ��r�Ĕ������£�
N2(g)+CO2(g) ��H= ��Q kJ��mol-1(Q>0)���_��ƽ��r�Ĕ������£�
�ضȣ��� | n (C)/mol | n(CO2)/mol |
T1 | 0.15 | |
T2 | 0.375 |
�������P�f�����_����
A. ��������Ϣ����֪��T1 > T2
B. T2���r���������_ƽ����ٿsС�������w�e��c (N2)��c (NO)����
C. T1���r�����_ʼ�r��������������pСһ�룬ƽ���NO���D��������
D. T1���r��ԓ������ƽ�ⳣ��![]()
�鿴�𰸺ͽ���>>
���H�WУ���x - �������б� - ԇ�}�б�
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^ | ����p�_�e�^ | ��vʷ̓�o���x�к���Ϣ�e�^ | �����֙��e�^
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com