
【題目】某實驗小組對氯水成分和性質進行研究,實驗如下:
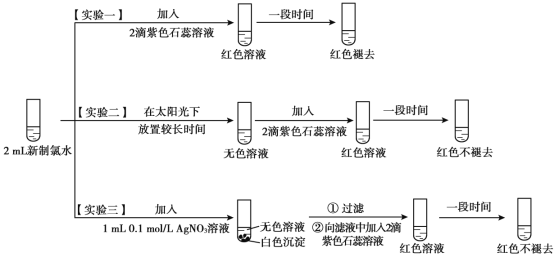
(1)氯水呈黃綠色,說明其中含有_________(填化學式)。
(2)實驗一的現象表明,氯水具有酸性和_________性。
(3)氯氣與水反應的化學方程式為__________。
(4)用化學用語說明實驗二中“紅色不褪去”的原因_______。
(5)實驗四證明了實驗三中“紅色不褪去”不是因為氯水被稀釋所致,補充所加試劑和現象。
(實驗四)
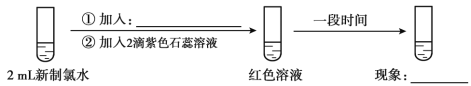
①加入:____________,現象:___________;
(6)進一步探究實驗三中“紅色不褪去”的原因。
(實驗五)取實驗三的白色沉淀,洗滌,用飽和氯化鈉溶液浸泡,取上層清液,滴加2滴紫色石蕊溶液,一段時間后,顏色褪去。寫出氯水和硝酸銀溶液反應的化學方程式______。
【答案】Cl2 漂白或氧化 Cl2 + H2O![]() HCl + HClO 2HClO
HCl + HClO 2HClO![]() 2HCl + O2↑ 1 mL蒸餾水 紅色褪去 Cl2 + 2AgNO3 + H2O =AgCl↓ + AgClO↓ + 2HNO3
2HCl + O2↑ 1 mL蒸餾水 紅色褪去 Cl2 + 2AgNO3 + H2O =AgCl↓ + AgClO↓ + 2HNO3
【解析】
氯氣溶于水發生反應Cl2+H2O![]() HCl+HClO,新制氯水含有Cl2、H2O、HClO、H+、Cl-、ClO—、OH—等粒子,能表現Cl2、HClO、H+、Cl-等微粒的性質。
HCl+HClO,新制氯水含有Cl2、H2O、HClO、H+、Cl-、ClO—、OH—等粒子,能表現Cl2、HClO、H+、Cl-等微粒的性質。
(1)氯水溶于水,溶于水的氯氣部分與水反應生成鹽酸和次氯酸,溶液呈黃綠色,說明溶液中含有Cl2分子,故答案為:Cl2;
(2)實驗一中加入石蕊試液變紅色,表明溶液呈酸性,溶液紅色褪去,說明氯水具有強氧化性而表現漂白性,故答案為:漂白或氧化;
(3)氯氣與水反應生成鹽酸和次氯酸,反應的化學方程式為Cl2 + H2O![]() HCl + HClO,故答案為:Cl2 + H2O
HCl + HClO,故答案為:Cl2 + H2O![]() HCl + HClO;
HCl + HClO;
(4)實驗二中新制氯水在太陽光下放置較長時間,次氯酸遇光分解生成鹽酸和氧氣,反應的化學方程式為2HClO![]() 2HCl + O2↑,故答案為:2HClO
2HCl + O2↑,故答案為:2HClO![]() 2HCl + O2↑;
2HCl + O2↑;
(5)由題意可知實驗四證明了實驗三中“紅色不褪去”不是因為氯水被稀釋,所以①加入1 mL蒸餾水,稀釋后繼續加入石蕊試液變紅色,一段時間后溶液紅色又褪去,故答案為:1 mL蒸餾水;紅色褪去;
(6)取實驗三的白色沉淀,洗滌,用飽和氯化鈉溶液浸泡,取上層清液,滴加2滴紫色石蕊溶液,一段時間后,顏色褪去說明白色沉淀中含有次氯酸銀沉淀,說明新制氯水與硝酸銀溶液反應生成氯化銀和次氯酸銀白色沉淀和硝酸,反應的化學方程式為Cl2 + 2AgNO3 + H2O =AgCl↓ + AgClO↓ + 2HNO3,故答案為:Cl2 + 2AgNO3 + H2O =AgCl↓ + AgClO↓ + 2HNO3。


 浙江之星課時優化作業系列答案
浙江之星課時優化作業系列答案 激活思維優加課堂系列答案
激活思維優加課堂系列答案科目:高中化學 來源: 題型:
【題目】過氧化鈣(CaO2)常用作種子及谷物的無毒性消毒劑,常溫下為白色的固體,微溶于水,且不溶于乙醇、乙醚和堿性溶液,但溶于酸。
某實驗小組擬探究CaO2的性質及其實驗室制法。
(1)實驗探究CaO2與酸的反應。
操作 | 現象 |
向盛有4 g CaO2的大試管中加入10mL稀鹽酸得溶液a | 劇烈反應,產生能使帶火星木條復燃的氣體 |
取5 mL溶液a于試管中,滴入兩滴石蕊試液 | 溶液變紅,一段時間后溶液顏色明顯變淺,稍后,溶液變為無色 |
①CaO2與鹽酸反應的化學方程式為_______________________________。
②加入石蕊試液后溶液褪色可能是因為溶液a中存在較多的_________。
(2)用如圖所示裝置制備過氧化鈣,其反應原理為Ca+O2![]() CaO2。
CaO2。
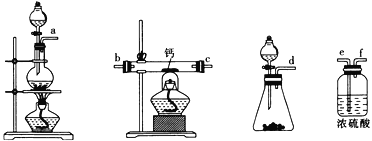
①請選擇實驗所需要的裝置,按氣流方向連接的順序為______________________(填儀器接口的字母,上述裝置可不選用也可重復使用)。
②根據完整的實驗裝置進行實驗,實驗步驟如下:Ⅰ.檢驗裝置的氣密性后,裝入藥品;Ⅱ.打開分液漏斗活塞,通入氣體一段時間,加熱藥品;Ⅲ.反應結束后,_________________________________(填操作);Ⅳ.拆除裝置,取出產物。
(3)利用反應:Ca2++ H2O2+2NH3+8H2O=CaO2·8H2O↓+2NH4+在堿性環境下制取CaO2的裝置如圖所示。

①NH3在Ca2+和H2O2的反應過程中所起的作用是______________________。
②反應結束后,經過濾、洗滌、低溫烘干可獲得CaO2·8H2O。過濾需要的玻璃儀器是_________;將沉淀進行洗滌的操作為_____________________________________________。
(4)設計實驗證明CaO2的氧化性比FeCl3的氧化性強:____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年是元素周期表誕生150周年,元素周期表(律)在學習、研究和生產實踐中有很重要的作用。下表為元素周期表的一部分,回答下列問題。
族 周期 | IA | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ||||||||
(1)元素①~⑧中,金屬性最強的是________(填元素符號)。
(2)中國青年化學家姜雪峰被國際組織推選為“元素⑦代言人”,元素⑦的原子結構示意圖是________,其氫化物的電子式是_________。
(3)元素①和②可以形成多種化合物。下圖模型表示的分子中,不可能由①和②形成的是_______(填序號)。
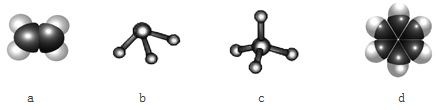
(4)比較元素②、③的最高價氧化物對應水化物的酸性:______>______(填化學式)。說明你判斷的理由:_________。
(5)主族元素砷(As)的部分信息如圖所示。
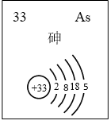
i.砷(As)在周期表中的位置是______。
ii.下列說法正確的是_______(填序號)。
a. 砷元素的最高化合價為+4
b. 推測砷有多種氧化物
c. ③的氣態氫化物的還原性大于砷的氣態氫化物的還原性
(6)某小組同學設計實驗比較VIIA元素的非金屬性:Cl>Br>I。
已知:常溫下濃鹽酸與高錳酸鉀反應生成氯氣。
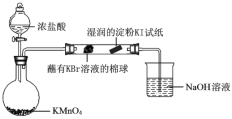
打開分液漏斗的活塞,燒瓶中產生黃綠色氣體,蘸有KBr溶液的棉球變為橙紅色,濕潤的淀粉KI試紙變藍,據此現象能否說明非金屬性:Br > I,并說明理由_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分枝酸可用于生化研究。其結構簡式如圖。下列關于分枝酸的敘述正確的是

A. 分子中含有2種官能團
B. 可與乙醇、乙酸反應,且反應類型相同
C. 1mol分枝酸最多可與3molNaOH發生中和反應
D. 可使溴的四氯化碳溶液、酸性高錳酸鉀溶液褪色,且原理相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知乙烯能發生以下轉化:

(1)乙烯的結構式為:___________________________________。
(2)寫出下列化合物官能團的名稱:
B中含官能團名稱________________;
D中含官能團名稱________________。
(3)寫出反應的化學方程式及反應類型:
①乙烯→B__________________;反應類型:________。
②B→C__________________;反應類型:________。
③B+D→乙酸乙酯_________________;反應類型:________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某恒溫密閉容器發生可逆反應Z(?)+W(?)![]() X(g)+Y(?) ΔH ,在t1時刻反應達到平衡,在t2時刻縮小容器體積,t3時刻再次達到平衡狀態后未再改變條件。下列有關說法中不正確的是( )
X(g)+Y(?) ΔH ,在t1時刻反應達到平衡,在t2時刻縮小容器體積,t3時刻再次達到平衡狀態后未再改變條件。下列有關說法中不正確的是( )
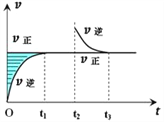
A. Z和W在該條件下一定不為氣態
B. t1~t2時間段與t3時刻后,兩時間段反應體系中氣體的平均摩爾質量不可能相等
C. 若在該溫度下此反應平衡常數表達式為K=c(X),則t1~t2時間段與t3時刻后的X濃度相等
D. 若該反應只在某溫度T0以上自發進行,則該反應的平衡常數K隨溫度升高而增大
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com